Methylmethaansulfonaat
| Methylmethaansulfonaat | |||||
|---|---|---|---|---|---|
| Structuurformule en molecuulmodel | |||||
| |||||
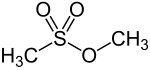
Structuurformule
| |||||
| |||||
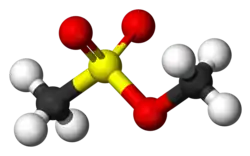
Ruimtelijk model
| |||||
| Algemeen | |||||
| Molecuulformule | |||||
| IUPAC-naam | Methylmethaansulfonaat | ||||
| Andere namen | Methaansulfonzuur methylester Methylmesylaat | ||||
| Molmassa | 110,13 g/mol | ||||
| SMILES | COS(=O)(=O)C
| ||||
| CAS-nummer | 66-27-3 | ||||
| EG-nummer | 200-625-0 | ||||
| PubChem | 4156 | ||||
| Wikidata | Q3077242 | ||||
| Waarschuwingen en veiligheidsmaatregelen | |||||
| |||||
| H-zinnen | H301 - H315 - H317 - H319 - H340 - H351 - H361 - H373 - H411[1] | ||||
| P-zinnen | P280 - P301+P330+P331 - P302+P352 - P305+P351+P338 - P308+P310 - P332+P313 | ||||
| Carcinogeen | ja | ||||
| EG-Index-nummer | 200-625-0 | ||||
| LD50 (ratten) | 225 mg/kg (oraal)[1] | ||||
| Fysische eigenschappen | |||||
| Dichtheid | 1,29 g/cm³ (20°C)[1] | ||||
| Smeltpunt | 20 °C[1] | ||||
| Kookpunt | 204 - 205 °C[1] | ||||
| Vlampunt | 104 °C[1] | ||||
| Dampdruk | 80 Pa[1] | ||||
| Oplosbaarheid in water | 200 g/L (20°C)[1] | ||||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | |||||
| |||||
Methylmetaansulfonaat (MMS), ook wel aangeduid als methylmesylaat is een organische verbinding met de brutoformule , wat met meer nadruk op de structuur van de verbinding geschreven kan worden als: . De verbinding is de methylester van methaansulfonzuur . De verbinding is een sterk methylerend reagens. Deze eigenschap maakt het tot een carcinogeen (zie hieronder) en waarschijnlijk ook een teratogeen. Ook op de huid heeft het een toxisch effect.[2] Hoewel zelf een carcinogeen wordt het ook ingezet bij de behandeling van sommige typen kanker.[3]
Chemische reacties met DNA
|
|
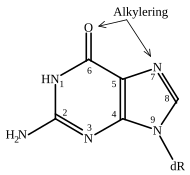
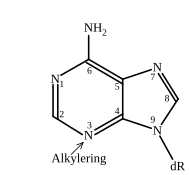
| Methylering guanine | Methylering adenosine |
| dR = Desoxyribose | |
MMS methyleert DNA voornamelijk op N7 in deoxyguanosine en op N3 in deoxyadenosine. Daarnaast zijn ook de andere zuurstof- en stikstof-atomen in DNA, in wel is waar veel mindere mate, evenals de niet aan koolstof gebonden zuurstof-atomen in de fosfaatbruggen, doelwit van methylering door MMS. Oorspronkelijk werd aangenomen dat MMS aanleiding zou geven tot breken van het dubbelstrengs DNA omdat homoloog recombinatie-deficiënte cellen veel gevoeliger zijn voor MMS.[4] Tegenwoordig wordt aangenomen dat MMS de voortgang van de replicatievork blokkeert.[4]
Zie ook
- Dimethylsulfiet, een structuurisomeer van MMS.
Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Methyl methanesulfonate op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ a b c d e f g h i (en) Gegevens van methylmethaansulfonaat in de GESTIS-stoffendatabank van het IFA (geraadpleegd op 18nfebruari 2025)
- ↑ Scorecard Pollution Information Site: Methyl Methanesulfonate Scorecard.org Accessed 14 Feb 08
- ↑ Methyl Methanesulfonate. Medical.Webends.com. Gearchiveerd op 15 februari 2008. Geraadpleegd op 14 februari 2008.
- ↑ a b Lundin, C, North M, Erixon K, Walters K, Jenssen D, Goldman AS, Helleday T (2005). Methyl methanesulfonate (MMS) produces heat-labile DNA damage but no detectable in vivo DNA double-strand breaks. Nucleic Acids Research 33 (12): 3799–3811. PMID 16009812. PMC 1174933. DOI: 10.1093/nar/gki681.


