Trifosfaan
| Trifosfaan | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
| ||||
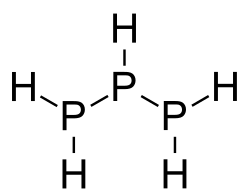
Structuurformule van trifosfaan
| ||||
| ||||
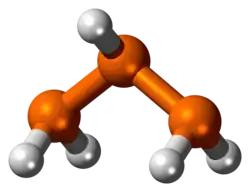
Ruimtelijk model van trifosfaan
| ||||
| Algemeen | ||||
| Molecuulformule | ||||
| IUPAC-naam | Trifosfaan[1] | |||
| Andere namen | Trifosfine[2] | |||
| Molmassa | 97,96099 g/mol | |||
| SMILES | PPP
| |||
| CAS-nummer | 13597-70-1 | |||
| PubChem | 139510 | |||
| Wikidata | Q1107689 | |||
| Beschrijving | Kleurloos gas | |||
| ||||
Trifosfaan (de systematische IUPAC-naam), of zoals het ook vaak genoemd wordt: trifosfine is een anorganische verbinding. De chemische formule voor deze stof is , of met meer nadruk op de structuur ervan, . Trifosfaan kan uit difosfaan gemaakt worden, maar is bij kamertemperatuur zeer instabiel.[3]
Naast de uitgangsstof is het trifosfaan ook verontreinigd met tetrafosfaan: of [4]
Met behulp van gaschromatografie zijn zuivere monsters verkregen. De stof ontleed echter snel tot fosfaan en cyclofosfaan, .[4]
Zie ook
Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Triphosphane op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
Externe links
Verwijzingen in de tekst
- ↑ triphosphane (CHEBI:35893). Chemical Entities of Biological Interest (ChEBI). European Bioinformatics Institute (7 June 2006). Geraadpleegd op 27 september 2011.
- ↑ Triphosphine. NIST Chemistry WebBook. National Institute of Standards and Technology. Geraadpleegd op 27 september 2011.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann. ISBN 978-0-08-037941-8.
- ↑ a b Marianne Baudler, Klaus Glinka (1993). Monocyclic and Polycyclic Phosphines. Chem.Rev. 93, pag.: 1623–1667. DOI: 10.1021/cr00020a010.