Partieel molair volume
Het partieel molaire volume ( of ) is een begrip uit de fysische chemie en thermodynamica en is gedefinieerd als de partiële afgeleide van het volume () van een mengsel naar de stofhoeveelheid () van een van de componenten in het mengsel.
Het partieel molaire volume van een bepaalde component in een systeem met meerdere componenten, zoals een oplossing of legering, is het (theoretische) aandeel dat deze component heeft in het totale volume:
en in het molaire volume:
met de stofhoeveelheidsfractie.
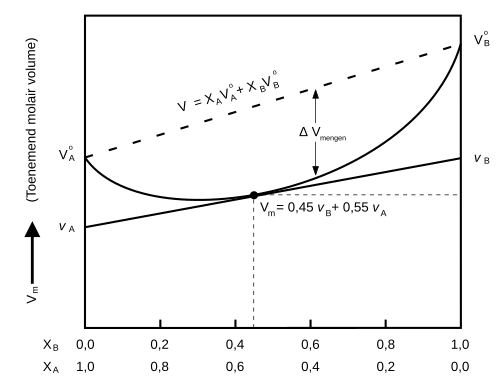
Omdat de intermoleculaire krachten tussen de verschillende componenten in het mengsel kunnen verschillen van de interacties in de ongemengde stoffen, kan er een verschil zijn tussen het partieel molaire volume van de componenten in het mengsel en het molaire volume van de zuivere stoffen. Hierdoor zal het totale volume van een oplossing verschillen van de opgetelde volumes van de verschillende zuivere componenten, wat ervoor zorgt dat bij het mengen bijvoorbeeld volumecontractie optreedt.