Glycerolcarbonaat
| Glycerolcarbonaat | ||||
|---|---|---|---|---|
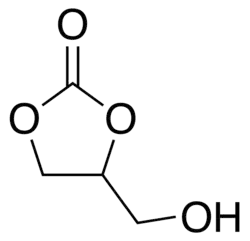
| Structuurformule en molecuulmodel | ||||
| ||||
Structuurformule van glycerolcarbonaat
| ||||
| Algemeen | ||||
| Molecuulformule | C4H6O4 | |||
| IUPAC-naam | 4-hydroxymethyl-1,3-dioxolan-2-on | |||
| Molmassa | 118 g/mol | |||
| SMILES | O=C1OCC(O1)CO
| |||
| InChI | 1S/C4H6O4/c5-1-3-2-7-4(6)8-3/h3,5H,1-2H2
| |||
| CAS-nummer | 931-40-8 | |||
| EG-nummer | 213-235-0 | |||
| PubChem | 97944 | |||
| Wikidata | Q5748964 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | vloeibaar | |||
| Kleur | kleurloos | |||
| Dichtheid | 1,4 g/cm³ | |||
| Smeltpunt | −69 °C | |||
| Kookpunt | 353,9 °C | |||
| Matig oplosbaar in | water | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Glycerolcarbonaat is een cyclische ester van waterstofcarbonaat (koolzuur) en glycerol. Het is bij omgevingstemperatuur een heldere vloeistof, die beneden −69 °C een glasachtige vaste stof wordt.
Synthese
Glycerolcarbonaat kan bereid worden door de rechtstreekse carbonylering van glycerol met waterstofcarbonaat.
Een andere mogelijkheid is de omestering van ethyleencarbonaat, di-ethylcarbonaat of dimethylcarbonaat met glycerol. Als katalysator wordt een base (natriumbicarbonaat of kaliumbicarbonaat) gebruikt.[1][2] Er bestaat ook de mogelijkheid om een lipase te gebruiken als biokatalysator.[3]
Glycerolcarbonaat ontstaat ook door de reactie van glycerol met ureum.[4][5]
Toepassingen
Glycerolcarbonaat heeft allerlei toepassingen, onder meer als monomeer voor polyesters, polycarbonaat, polyamide of polyurethaan. Het wordt verder ingezet als oplosmiddel voor chemische reacties of voor elektrolyt in batterijen, als chemisch intermediair en als additief in oppervlakteactieve stoffen en smeeroliën. Het is een groen oplosmiddel in die zin dat het geen gevaarlijke stof is en dat het uit hernieuwbare grondstoffen kan bereid worden; glycerol is een bijproduct van de biodieselproductie. Verder is het ook gemakkelijk biodegradeerbaar, vanwege de esterfunctionaliteit.
Glycerolcarbonaat wordt gebruikt als emulgator in cosmetica en was- en reinigingsmiddelen. Het heeft daarenboven een glansverschaffend effect (lustering of avivage genoemd).[6]
Glycerolcarbonaat kan gemakkelijk omgezet worden in glycidol en koolstofdioxide door verhitting in aanwezigheid van een metaalzout als natriumfosfaat of calciumcarbonaat.[7]
Externe links
- (en) ChemSpider CSID: 88417
- (en) JEFFSOL Carbonates[dode link]
- ↑ (en) U.S. Patent 2915529, "Method for preparing glycerin carbonate" van 1 december 1959 aan Jefferson Chemical Company
- ↑ (en) Y. Patel, J. George, S.M. Pillai & P. Munshi (2009) - Effect of liophilicity of catalyst in cyclic carbonate formation by transesterification of polyhydric alcohols, Green Chem., 11, pp. 1056-1060
- ↑ (en) U.S. Patent 8314259, "Method of manufacturing glycerol carbonate" van 20 november 2012 aan GS Caltex Corp.
- ↑ (en) U.S. Patent 6025504, "Method for preparing glycerol carbonate" van 15 februari 2000 aan Organisation Nationale Interprofessionnelle des Oleagineux (Frankrijk)
- ↑ (en) M.J. Climent, A. Corma, P. De Frutos, S. Iborra, M. Noy, A. Velty & P. Concepción (2010) - Chemicals from biomass: Synthesis of glycerol carbonate by transesterification and carbonylation with urea with hydrotalcite catalysts. The role of acid–base pairs, Journal of Catalysis, 269, pp. 140–149
- ↑ (de) Duits octrooi 19756454, "Verwendung von Glycerincarbonat" van 17 juni 1999 aan Cognis Deutschland GmbH
- ↑ (en) U.S. Patent 2856413, "Method for preparing glycidol" van 14 oktober 1958 aan Jefferson Chemical Company