Chlorylfluoride
| Chlorylfluoride | ||||
|---|---|---|---|---|
| Structuurformule en molecuulmodel | ||||
| ||||
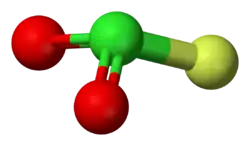
Molecuulmodel van chlorylfluoride
| ||||
| Algemeen | ||||
| Molecuulformule | FClO2 | |||
| Molmassa | 86,450203 g/mol | |||
| SMILES | O=Cl(=O)F
| |||
| InChI | 1S/ClFO2/c2-1(3)4
| |||
| CAS-nummer | 13637-83-7 | |||
| PubChem | 139523 | |||
| Wikidata | Q1916758 | |||
| Fysische eigenschappen | ||||
| Aggregatietoestand | gasvormig | |||
| Dichtheid | 3,534 g/cm³ | |||
| Smeltpunt | −15 °C | |||
| Kookpunt | −6 °C | |||
| Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C, 1 bar). | ||||
| ||||
Chlorylfluoride een anorganische verbinding van chloor, fluor en zuurstof, met als brutoformule FClO2. Het is het zuurfluoride van waterstofchloraat. De structuur van de molecule wordt voorspeld door de VSEPR-theorie en is trigonaal piramidaal.
Synthese
Chlorylfluoride werd voor het eerst bereid in 1942 door Schmitz & Schumacheb door fluorering van chloordioxide.[1] Tegenwoordig wordt de verbinding gesynthetiseerd uit reactie van natriumchloraat en chloortrifluoride:
Zie ook
Bronnen, noten en/of referenties
- ↑ (de) H. Schmitz, H.J. Schumacheb - Über eine neue Reaktion des Chlordioxyds. Die Bildung einer Verbindung der Formel ClO2F[dode link], Zeitschrift für anorganische und allgemeine Chemie, Volume 249, pp. 238-244 (1942)