Amniotische epitheliale stamcel
.jpg)

Een amniotische epitheliale stamcel (AESC) of amniotische epitheelcel is een type stamcel afgeleid van het binnenmembraan van de placenta. Epitheelcellen afkomstig van amnioblasten beginnen zich ongeveer 8 dagen na de bevruchting te ontwikkelen. Het is bekend dat deze cellen dezelfde markers tot expressie brengen als embryonale stamcellen, met name Oct-4 en nanog. Deze transcriptiefactoren bepalen de pluripotentie van stamcellen.[1][2] Amniotische epitheliale stamcellen hebben het vermogen om alle drie de kiembladen te vormen: endoderm, mesoderm en ectoderm.[3][4] Vanwege de pluripotentie van menselijke amniotische epitheliale stamcellen is het mogelijk om ze te gebruiken voor de behandeling van ziekten en aandoeningen van het zenuwstelsel en andere weefsels. Kunstmatige hartkleppen en werkende luchtpijpen, evenals spier-, vet-, zenuw-, bot- en levercellen zijn gemaakt met behulp van amniotische epitheliale stamcellen.[5][6] Weefsels afkomstig van amniotische epitheliale stamcellijnen lijken veelbelovend voor patiënten met aangeboren aandoeningen of misvormingen van het hart, de lever, de longen, de nieren en het hersenweefsel.
Transplantatie
Amniotische epitheliale stamcellen blijken veilig en succesvol getransplanteerd te kunnen worden naar patiënten die niet verwant zijn aan de donor. Een mogelijke reden hiervoor is dat amniotische epitheliale stamcellen lage antigeenniveaus hebben die de compatibiliteit van een donor met de ontvanger belemmeren. Dit maakt de kans op afstoting van de cellen door het ontvangende weefsel kleiner. In tegenstelling tot traditionele weefseltransplantaties, waarbij de donor en de ontvanger volledig synchroon moeten zijn wat betreft bloedgroep en algehele compatibiliteit en zelfs nog steeds weefselafstoting kunnen vertonen, kunnen amniotische epitheliale stamcellen worden gebruikt en vertonen ze een grotere kans op weefselacceptatie. Ook is bekend dat amniotische epitheliale stamcellen natuurlijke wondgenezing bevorderen en de angiogenese remmen, wat de basisconversie is van een tumor naar kwaadaardige kanker.
Voordelen ten opzichte van embryonale stamcellen
Bij het oogsten van embryonale stamcellen wordt een menselijk embryo vernietigd. Veel anti-abortusindividuen associëren deze handeling met abortus en beschouwen het als immoreel. Amniotische epitheliale stamcellen worden geoogst uit de placenta, die doorgaans na de geboorte wordt weggegooid.[7] De cellen zijn zeer eenvoudig te verkrijgen zonder het gebruik van ingrijpende procedures. Hun gebruik voorkomt dus de controverse over embryonale stamcellen. Er worden grote hoeveelheden amniotische epitheliale stamcellen gevonden in de placenta en er kunnen bij één extractie meer dan 50-100 miljoen cellen worden verkregen. Er zijn echter meerdere miljarden cellen nodig voor transplantatie om ziekten te behandelen en te bestrijden. Daarom moeten de cellen in een laboratorium worden vermeerderd om voldoende cellen voor transplantatie te krijgen.
In tegenstelling tot embryonale stamcellen hebben amniotische epitheliale stamcellen geen neiging getoond om zich te ontwikkelen tot teratomen en andere kankerachtige tumoren bij injectie in levend weefsel. Amniotische epitheliale stamcellen staan niet bekend om kankerachtige tumoren te produceren in de gastheer, ondanks het feit dat deze cellen wel genen tot expressie brengen die worden aangetroffen in embryonale stamcellen waarvan bekend is dat ze tumorvorming bevorderen.
Organen die zijn gemaakt uit amniotische epitheliale stamcellen verkregen uit de placenta van de patiënt, die getransplanteerd wordt, zouden bij transplantatie niet door die patiënt worden afgestoten. Dergelijke organen hebben hetzelfde genotype en zijn dus volledig compatibel met het immuunsysteem van die patiënt.
Vermeerdering
Omdat er niet voldoende amniotische epitheliale stamcellen uit een enkele placenta kunnen worden gehaald om te worden gebruikt in cellulaire therapieën, moeten de cellen in een laboratorium worden vermeerderd. Sommige onderzoeken hebben echter aangetoond dat zodra deze cellen in het laboratorium worden vermeederd, een deel van de pluripotentie verloren gaat. Ook hebben deze in het laboratorium gekweekte cellen een veranderde genexpressie laten zien, wat leidt tot een verschillend fenotype en verschillende antigeenniveaus. Dit kan hun vermogen om compatibel te zijn met niet-gerelateerde weefsels veranderen. Veel van de effecten van het vermeerderen van deze cellen zijn onbekend en onderzoekers blijven manieren zoeken om deze cellen te kweken zonder hun pluripotente eigenschappen te veranderen. Onderzoekers hebben ontdekt dat het invriezen van amniotische epitheliale stamcellen ervoor zorgt dat ze niet functioneren zoals ze normaal zouden doen, waardoor onderzoekers denken dat de extracellulaire matrix het deel van de cel is dat zijn functies controleert.
Stamceltherapieën

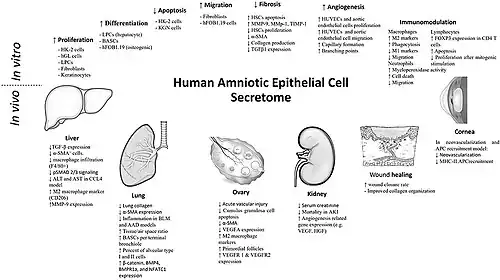
Er zijn verschillende onderzoeken uitgevoerd naar de potentiële voordelen van het gebruik van amniotische epitheliale stamcellen in verschillende delen van het lichaam. Een mogelijk gebruik van deze cellen omvat stamceltherapieën gericht op het verminderen van ontstekingen en littekens. Modellen hebben aangetoond dat het gebruik van deze cellen om dergelijke ontstekingen te verminderen, lonende effecten heeft gehad in de longen en de lever. Meer specifiek zijn amniotische epitheliale stamcellen in het verleden gebruikt om genetische leverziekten te behandelen, zoals ornithinetranscarbamylasedeficiëntie, familiaire hypercholesterolemie en het syndroom van Crigler-Najjar. Deze cellen worden door onderzoekers gezien als een nieuwe en efficiëntere manier om leverziekten te behandelen, met name vanwege het probleem dat voortkomt uit een gebrek aan leverdonoren. Onderzoekers werken ook met genetisch gemodificeerde menselijke amniotische epitheliale stamcellen in nieuwe experimentele procedures en stamceltherapieën.
Ook hebben amniotische epitheliale stamcellen potentie getoond om weefselherstel van de ontvanger te stimuleren. Studies hebben aangetoond dat het gebruik van amniotische epitheliale stamcellen in stamceltherapieën met betrekking tot letsels aan het ruggenmerg veelbelovend is vanwege hun vermogen om te differentiëren tot volledig operationele zenuwcellen en neurotransmitters vrij te geven. Deze cellen kunnen ook worden gebruikt om ziekten te behandelen die het centraal zenuwstelsel aantasten, evenals andere neurologische aandoeningen.
Amniotische epitheliale stamcellen kunnen acetylcholine en catecholamine aanmaken en vrijgeven. Ze vertonen ook genexpressie voor dopaminereceptoren en -transporters. Om deze reden worden ze ook bestudeerd door onderzoekers die de effecten van nieuwe medicijnen op dopaminereceptoren en -transporters onderzoeken, evenals de basisfuncties, waaronder dopamineafscheiding en -opname. Verschillende onderzoekers hebben geconcludeerd dat deze cellen, bij transplantatie op laboratoriumratten met de ziekte van Parkinson, de effecten van de ziekte omkeerden door de dopamine-afgevende zenuwcellen te vervangen die waren afgestorven en te voorkomen dat andere zenuwcellen door de ziekte werden vernietigd.[8] Momenteel wordt de ziekte van Parkinson behandeld met dopaminevervangingstherapie, maar is niet functioneel bij de late progressie van de ziekte en kan de ziekte niet genezen. Ook andere cellen die in het verleden zijn gebruikt voor transplantatie om de ziekte van Parkinson te behandelen, zoals neurale stamcellen en embryonale stamcellen, zijn beperkt of controversieel in hun terugwinning. Soortgelijke positieve effecten zijn ook aangetoond in onderzoeken met kippen met neurologische aandoeningen.
Experimenten met laboratoriummuizen hebben geconcludeerd dat amniotische epitheliale stamcellen ook kunnen differentiëren tot cellen van de alvleesklier die insuline produceren en de bloedglucosespiegel reguleren. Dit zou een mogelijke genezing of behandeling kunnen zijn voor diabetes van beide typen.
Deze stamcellen kunnen ook in de longen worden gebruikt omdat ze kunnen differentiëren tot cellen (pneumocyten) die oppervlakte-actieve stof produceren, wat de longontwikkeling bij foetussen bevordert. Dit zou kunnen worden gebruikt als behandeling voor te vroeg geboren baby's met een onderontwikkelde longcapaciteit. Een ander veelbelovend gebruik van amniotische epitheliale stamcellen is om ze op het hoornvlies aan te brengen om de functie ervan te herstellen bij personen met hoornvliesfalen. Onderzoeken hebben aangetoond dat wanneer deze cellen worden aangebracht, het de zwelling van het oculaire vlak vermindert.[9] Amniotische epitheliale stamcellen hebben ook positieve effecten laten zien bij gebruik om ernstige brandwondenslachtoffers te behandelen door weefselherstel van de ontvanger te stimuleren en als behandeling voor bepaalde auto-immuunziekten.
Onderzoekers van de Kyoto Prefectural University of Medicine hebben een onderzoek uitgevoerd waarin ze amniotische epitheliale stamcellen in de mondholte transplanteerden om orale mucosale defecten (mondslijmvliesontstekingen) te behandelen. Omdat huidtransplantaten die uit de mondholte worden genomen defecten op de donorplaats veroorzaken, zochten wetenschappers naar een betere manier om deze defecten te behandelen zonder defecten door transplantatie te veroorzaken. Deze onderzoekers gebruikten laboratoriumkonijnen met orale mucosale defecten en transplanteerden gekweekte amniotische epitheliale stamcellen naar de defecte gebieden. De gekweekte amniotische epitheliale stamcellen vertoonden markers die op de orale mucosale cellen werden aangetroffen, zoals bepaalde keratines. Ze ontdekten dat de amniotische epitheliale stamcellen zich differentieerden in mucosale-achtige cellen en op het mucosale defect bleven en daarom een mogelijk mechanisme zouden kunnen zijn voor de behandeling van die defecten.[10] Onderzoekers hebben onlangs ontdekt dat menselijke amniotische epitheliale stamcellen in staat zijn om het bloedplasma-proteïne albumine te produceren en vrij te geven.[11]
Externe links
- Human Amniotic Epithelial Cells Catalog #7110 at ScienCell Research Laboratories, inc.
- Gita Pratama (July 26, 2011). Changes in Culture Expanded Human Amniotic Epithelial Cells: Implications for Potential Therapeutic Applications. PLOS ONE 6 (11): e26136. PMID 22073147. PMC 3206797. DOI: 10.1371/journal.pone.0026136.
- Hodges Alex (August 20, 2020). Human Amnion Epithelial Cells Produce Soluble Factors that Enhance Liver Repair by Reducing Fibrosis While Maintaining Regeneration in a Model of Chronic Liver Injury. Cell Transplantation 29. PMID 32813573. PMC 7563845. DOI: 10.1177/0963689720950221.
- Andrewartha, Neil, Yeoh, George (7 August 2019). Human Amnion Epithelial Cell Therapy for Chronic Liver Disease. Stem Cells International 2019: 8106482. PMID 31485235. PMC 6702811. DOI: 10.1155/2019/8106482.
- Haochuan Li (July 4, 2004). Immunosuppressive Factors Secreted by Human Amniotic Epithelial cells. Investigative Ophthalmology & Visual Science 46 (3): 900–7. PMID 15728546. DOI: 10.1167/iovs.04-0495.
- Norio Sakuragawa (January 31, 2000). Human Amniotic Epithelial cells are promising transgene carriers for Allogenic Cell transplantation. Journal of Human Genetics 45 (3): 171–176. PMID 10807543. DOI: 10.1007/s100380050205. Geraadpleegd op 9 april 2012.
- Rick Weiss, "Scientists See Potential In Amniotic Stem Cells", 8 januari 2007. Geraadpleegd op 31 juli 2010.
- Sankar Venkatachalam (19 april 2009). Novel neurotrophic factor secreted by amniotic epithelial cells. Biocell 33 (2): 81–89. PMID 19886035. DOI: 10.32604/biocell.2009.33.081. Geraadpleegd op 9 april 2012.
- Toshio Miki (1 november 2005). Stem Cell Characteristics of Amniotic Epithelial Cells. Stem Cells 23 (10): 1549–1559. PMID 16081662. DOI: 10.1634/stemcells.2004-0357.
Dit artikel of een eerdere versie ervan is een (gedeeltelijke) vertaling van het artikel Amniotic epithelial cell op de Engelstalige Wikipedia, dat onder de licentie Creative Commons Naamsvermelding/Gelijk delen valt. Zie de bewerkingsgeschiedenis aldaar.
- ↑ Bilic, G, Zeisberger, SM, Mallik, AS, Zimmermann, R, Zisch, AH (2008). Comparative characterization of cultured human term amnion epithelial and mesenchymal stromal cells for application in cell therapy.. Cell transplantation 17 (8): 955-68. PMID 19069637. DOI: 10.3727/096368908786576507. Geraadpleegd op 22 november 2019.
- ↑ Miki, T, Lehmann, T, Cai, H, Stolz, DB, Strom, SC (NaN). Stem cell characteristics of amniotic epithelial cells.. Stem cells (Dayton, Ohio) 23 (10): 1549-59. PMID 16081662. DOI: 10.1634/stemcells.2004-0357. Geraadpleegd op 22 november 2019.
- ↑ Ilancheran, S, Michalska, A, Peh, G, Wallace, EM, Pera, M (2007-09). Stem cells derived from human fetal membranes display multilineage differentiation potential.. Biology of reproduction 77 (3): 577-88. PMID 17494917. DOI: 10.1095/biolreprod.106.055244. Geraadpleegd op 22 november 2019.
- ↑ Pratama, G, Vaghjiani, V, Tee, JY, Liu, YH, Chan, J (2011). Changes in culture expanded human amniotic epithelial cells: implications for potential therapeutic applications.. PloS one 6 (11): e26136. PMID 22073147. DOI: 10.1371/journal.pone.0026136. Geraadpleegd op 22 november 2019.
- ↑ Fang, CH, Jin, J, Joe, JH, Song, YS, So, BI (2012). In vivo differentiation of human amniotic epithelial cells into cardiomyocyte-like cells and cell transplantation effect on myocardial infarction in rats: comparison with cord blood and adipose tissue-derived mesenchymal stem cells.. Cell transplantation 21 (8): 1687-96. PMID 22776022. DOI: 10.3727/096368912X653039. Geraadpleegd op 22 november 2019.
- ↑ Zhu, S, Li, J, Zhu, Q, Dai, T, He, B (2015-02). Differentiation of human amniotic epithelial cells into Schwann‑like cells via indirect co‑culture with Schwann cells in vitro.. Molecular medicine reports 11 (2): 1221-7. PMID 25374158. DOI: 10.3892/mmr.2014.2881. Geraadpleegd op 22 november 2019.
- ↑ Byron Spice, Option to stem cells found. www.postgazette.com (August 5, 2005). Gearchiveerd op 20 August 2010. Geraadpleegd op 31 juli 2010.
- ↑ Yang Xin-xin, Therapeutic effect of human amniotic epithelial cell transplantation into the lateral ventricle of hemiparkinsonian rats (2009). Geraadpleegd op 9 april 2012.
- ↑ Transplantation of Tissue Cultured Human Amniotic Epithelial Cells Onto Damaged Ocular Surfaces. ClinicalTrials.gov. Geraadpleegd op 31 juli 2010.
- ↑ Takeshi Amemiya (January 21, 2010). Immunohistochemical study of Oral Epithelial sheets Cultured on Amniotic Membrane for Oral Mucosal Reconstruction. Biomed Mater Eng 20 (1): 37–45. PMID 20448302. DOI: 10.3233/BME-2010-0613.
- ↑ Yonathan Garfias (October 2010). Amniotic Membrane is an Immunosuppressor of Peripheral Blood Mononuclear Cells. Immunol Invest 40 (2): 183–96. PMID 21080833. DOI: 10.3109/08820139.2010.532266.